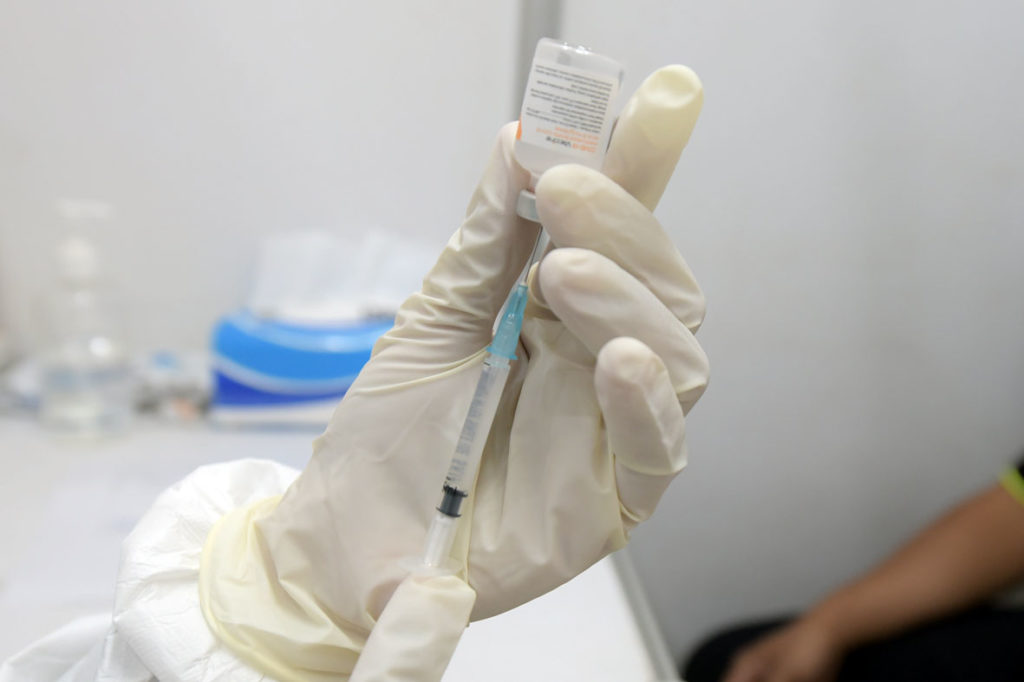
Badan Pengawas Obat dan Makanan (BPOM) telah menerbitkan izin penggunaan darurat atau emergency use authorization untuk vaksin COVID-19 produksi dalam negeri, yaitu Vaksin Indovac, pada tanggal 24 September 2022.
“Sudah mendapatkan emergency use authorization yaitu pertama adalah Vaksin Indovac. Ini adalah vaksin yang merupakan pengembangan dalam negeri,” ujar Kepala BPOM Penny K. Lukito dalam keterangan pers, Jumat (30/09/2022).
Penny menjelaskan, Vaksin Indovac dengan kandungan zat aktif rekombinan Receptor-Binding Domain (RBD) protein S virus SARS-Cov-2, merupakan vaksin COVID-19 dengan platformrekombinan protein subunit yang dikembangkan oleh PT Bio Farma bekerja sama dengan Baylor College of Medicine, Amerika Serikat.
Pada waktu bersamaan BPOM juga menerbitkan EUA untuk Vaksin AWcorna. Vaksin COVID-19 dengan platform mRNA ini didaftarkan oleh PT Etana Biotechnologies Indonesia (PT Etana) dan dikembangkan oleh Abogen-Yuxi Walvax, Cina.
Kepala BPOM mengharapkan dengan disetujuinya EUA terhadap kedua vaksin ini, semakin menambah alternatif vaksin yang dapat digunakan dalam program vaksinasi COVID-19 untuk dewasa usia 18 tahun ke atas serta mendukung kemandirian vaksin Indonesia.
“Dengan telah diterbitkannya EUA kemudian ada alternatif jenis vaksin untuk penanggulangan COVID-19 yang saya kira masih panjang waktunya ke depan. Juga tentunya untuk aspek kemandirian vaksin dan tidak hanya mencukupi kebutuhan domestik dengan produksi vaksin dalam negeri tetapi juga untuk produk kita sebagai produk ekspor,” ujarnya.
Lebih lanjut, Penny menyampaikan bahwa kedua vaksin ini juga telah mendapatkan sertifikat halal dari Majelis Ulama Indonesia (MUI).
“Kedua vaksin ini telah mendapatkan fatwa halal dari MUI dan sertifikasi halal dari Badan Penyelenggara Jaminan Produk Halal (BPJPH),” tandasnya. (HUMAS BPOM/UN)